4月10日-15日,第112屆美國癌癥研究協會(AACR)年會以虛擬會議形式舉行。貝達藥業甲磺酸貝福替尼(BPI-D0316)二線臨床研究數據在會議上亮相。

表皮生長因子受體(EGFR)是一種廣泛存在于人體表皮細胞和基質細胞的具有酪氨酸激酶活性的膜表面受體。在正常細胞中,EGFR酪氨酸激酶(EGFR-TK)受其配體調控,發揮著正常的細胞生長、增殖等功能。當該通路的調控基因出現突變或者擴增時,則可使其介導的下游通路異常激活,從而誘發多種癌癥。
在EGFR突變陽性非小細胞肺癌(NSCLC)患者中,使用第一代表皮生長因子受體酪氨酸激酶抑制劑(EGFR-TKI)后,超過半數會發生T790M突變并耐藥,因此針對克服T790M耐藥突變的第三代EGFR-TKI應運而生。甲磺酸貝福替尼是一種新型的第三代EGFR-TKI,能夠選擇性地抑制EGFR T790M突變,擬用于治療攜帶EGFR敏感性突變或使用EGFR-TKI耐藥后產生T790M突變的非小細胞肺癌患者。
本研究為多中心、開放、單臂II期臨床研究,評估研究藥物在既往接受一代或二代EGFR-TKI治療后產生耐藥且EGFR-T790M突變陽性的局部晚期或轉移性NSCLC患者中的療效和安全性。
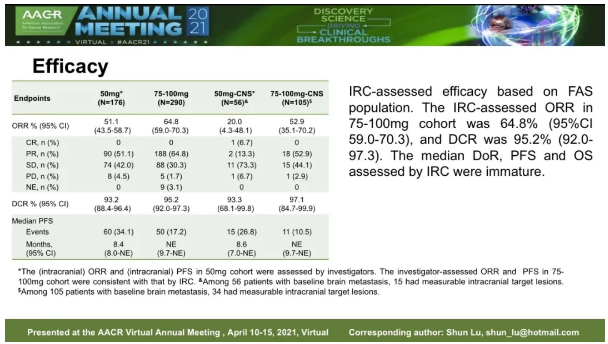
研究由上海市胸科醫院陸舜教授牽頭開展,全國共計51家研究中心參與,共納入了176例受試者至50mg劑量組,290例受試者至75-100mg劑量組。75-100mg劑量組受試者先經甲磺酸貝福替尼75mg QD治療21天作為導入期,若耐受性良好,則升高劑量至100mg QD。截至2020年10月18日數據顯示甲磺酸貝福替尼膠囊75-100mg治療既往使用EGFR-TKI耐藥后產生T790M突變的局部晚期或轉移性非小細胞肺癌患者,188例患者經獨立評審委員會(IRC)評估確認為PR,客觀緩解率(ORR)為64.8%(95%CI:59.0-70.3) ,疾病控制率 (DCR) 為 95.2% (95% CI: 92.0-97.3)。34例基線有腦轉移的患者中, 18例經IRC評估確認為PR ,顱內客觀緩解率(iORR) 為52.9% (95% CI: 35.1-70.2),顱內疾病控制率(iDCR)為97.1%。PFS,DoR,OS尚未成熟。最常見的不良反應為血小板減少癥(57.2%)、頭痛(27.6%)、白細胞計數降低(23.4%)、貧血(22.1%)、皮疹(20.7%)。最常見的嚴重程度≥3級不良反應為血小板減少癥(11.7%)。
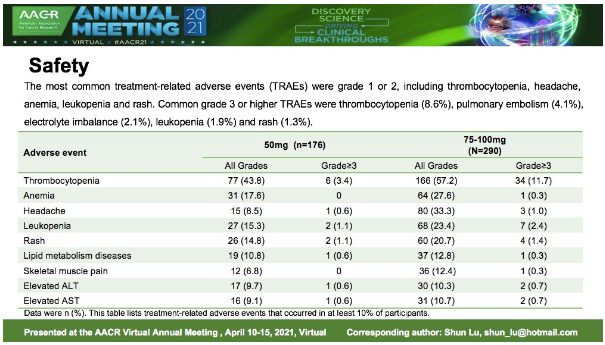
貝達藥業副總裁兼臨床管理和醫學事務負責人季東表示,甲磺酸貝福替尼膠囊75-100mg治療既往使用EGFR-TKI耐藥后產生T790M突變的局部晚期或轉移性NSCLC患者具有較好的療效和安全性,可為EGFR-TKI耐藥后產生T790M突變的NSCLC患者提供新的有效的治療選擇。目前,甲磺酸貝福替尼膠囊上市許可申請已獲受理。期待甲磺酸貝福替尼能夠早日獲批上市,盡早造福患者。
關于AACR年會
美國癌癥研究協會(AACR)年會是全球歷史最悠久、規模最大的腫瘤研究學術會議之一。會議關注高質量腫瘤研究及創新的各個方面,是全球腫瘤研究的焦點,將匯集腫瘤領域的最前沿的研究成果。今年會議的主題是“發現科學推動臨床突破”。
下一條: 浙江省委統戰部副部長、省工商聯黨組書記陳浩一行調研貝達夢工場
