近日,美國C4 Therapeutics,Inc.(C4T)宣布申報的 CFT8919藥品臨床試驗申請獲美國食品藥品監督管理局批準。CFT8919由貝達藥業與C4T在中國(包括香港、澳門和臺灣地區)聯合開發,是一種口服生物可利用的 BiDAC? 降解劑,旨在針對非小細胞肺癌 (NSCLC) 患者有效和選擇性地對抗 EGFR L858R。
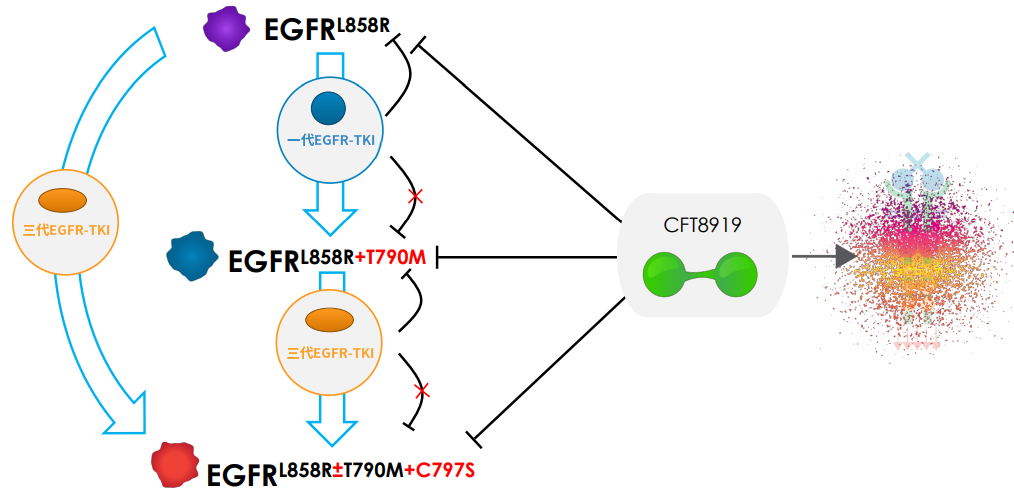
△CFT8919作用機理圖(來源:C4T)
CFT8919在EGFR L858R驅動的NSCLC的體內外模型中具有活性,可靶向廣泛的在靶耐藥突變并有顱內活性,具有預防或治療患者腦轉移的潛力。CFT8919通過與L858R突變的變構位點結合,展示出良好的選擇性,同時對像T790M或C797S突變的EGFR繼發耐藥突變有效。此外,CFT8919不僅對攜帶L858R單突變而且對奧希替尼、厄洛替尼耐藥后產生的L858R繼發耐藥突變,均具有很好細胞增殖抑制活性,同時展示出良好的EGFR野生型選擇性。
貝達藥業董事長丁列明表示,CFT8919是貝達繼一代、三代、四代小分子及EGFR/cMET雙抗后,在EGFR通路布局的另一重要補充,也是公司第一個靶向蛋白降解藥物。亞洲EGFR L858R突變患病人群較多,存在較大的未被滿足的臨床用藥需求,CFT8919在全球屬于技術領先的藥物,期望在中國早日開展臨床研究,為EGFR L858R突變患者提供新的治療選擇。
關于C4 Therapeutics
C4 Therapeutics (C4T)是一家致力于靶向蛋白質降解科學研究的生物制藥公司,專注創造改變患者生活的新一代藥物。C4T正在利用其TORPEDO?平臺有效地設計和優化小分子藥物,利用人體的天然蛋白質回收系統快速降解致病蛋白質,從而有可能克服耐藥性。C4T正在推進多個靶向腫瘤學項目至臨床階段,并擴大其研究平臺,為難以治療的疾病提供更多藥物。
下一條: 美納五福,賽贏未來|賽美納、伏美納上市會在杭舉行
