近日,貝達藥業收到國家藥品監督管理局簽發的《藥品注冊證書》(藥品批準文號:國藥準字H20230011、H20230012),甲磺酸貝福替尼膠囊(賽美納?)適用于“具有表皮生長因子受體(EGFR)外顯子19缺失或外顯子21(L858R)置換突變的局部晚期或轉移性非小細胞肺癌(NSCLC)成人患者的一線治療”適應癥獲批上市。這是甲磺酸貝福替尼膠囊獲批的第二項適應癥。
甲磺酸貝福替尼膠囊是針對T790M突變的第三代EGFR-TKI,具有巨大的臨床需求。既往臨床研究數據被《柳葉刀· 呼吸醫學》在編者按中評價:貝福替尼作為EGFR突變的晚期非小細胞肺癌的新候選藥物,可作為中國患者新的用藥選擇。
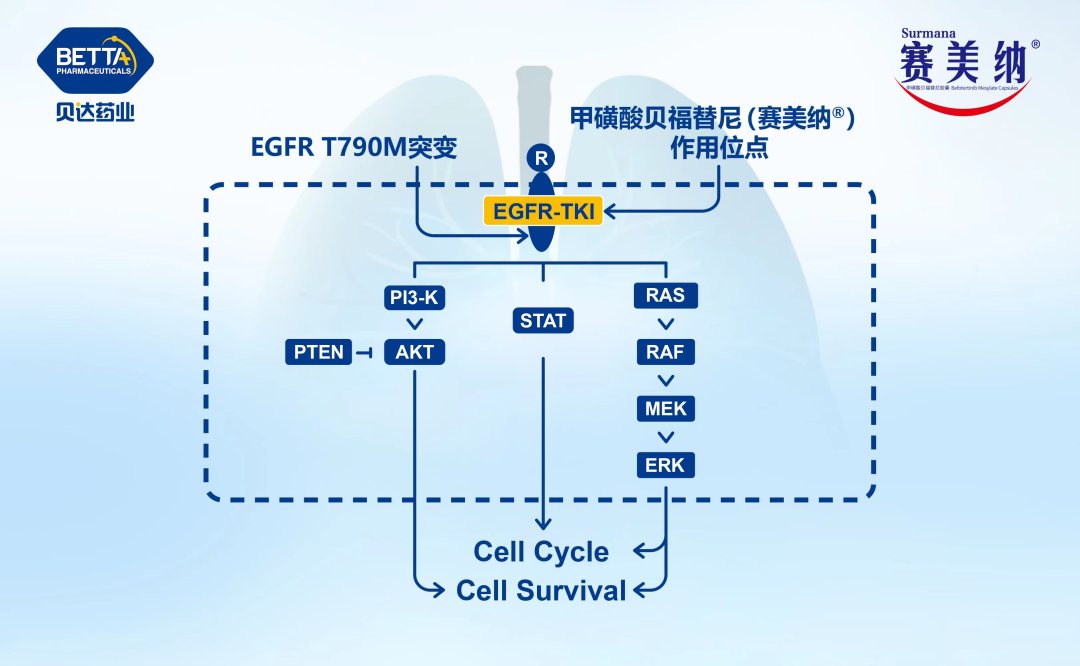
△甲磺酸貝福替尼膠囊作用機理圖
本次新適應癥獲得批準是基于一項隨機、對照、多中心、開放性的II/III期研究(IBIO-103),在既往未接受過系統治療的EGFR敏感突變陽性的局部晚期或轉移性NSCLC患者中,評價貝福替尼(75→100 mg)對比埃克替尼(125 mg)的有效性和安全性。研究共納入362名患者,按1:1隨機化分組到貝福替尼組或埃克替尼組。貝福替尼組和埃克替尼組IRC評估的中位PFS分別為22.1個月和13.8個月(HR 0.49, P<0.0001),相較于埃克替尼,貝福替尼可降低51%的疾病進展或死亡風險。在基線腦轉移患者中,貝福替尼仍可降低52%的疾病進展或死亡風險(HR 0.48, P=0.0086)。安全性方面,治療相關的不良事件(TRAEs)主要為1~2級,血小板減少是最常見的TRAE。試驗過程中未觀察到新的安全性信號。
貝達藥業副總裁王三虎表示,國家藥品監督管理局對貝福替尼一線適應癥的批準不僅是對其臨床效果和安全性的進一步認可,也是對中國創新藥物研發的鼓勵和支持。期待貝福替尼在未來能夠幫助更多的肺癌患者戰勝病魔,重獲新生。
項目主要研究者、上海市胸科醫院陸舜教授表示,貝福替尼一線適應癥的獲批,為醫生提供了新的治療武器,將提升晚期肺癌患者生存質量。期待貝福替尼開展更多臨床研究,累積更多臨床數據,為中國患者提供更好的治療指導。
貝達藥業董事長丁列明博士表示,貝福替尼一線適應癥的獲批,離不開監管部門和臨床專家長期的支持與幫助,是公司多部門通力協作、辛勤付出的結果,更是貝達在肺癌創新藥領域的堅守和傳承。期待貝福替尼為更多非小細胞肺癌患者帶來福音,公司將繼續堅持醫藥創新,做更多老百姓用得起的新藥好藥。
下一條: 貝達藥業注射用MCLA-129和甲磺酸貝福替尼膠囊聯合研究首例受試者入組
