9月2日,貝達藥業股份有限公司發布公告,因公司新藥鹽酸恩沙替尼(X-396)在臨床研究中表現出來持續的治療效果,近期經獨立評審委員會(IRC)對截至2019年5月底的最新數據進行評估,更新鹽酸恩沙替尼藥品注冊臨床試驗數據。
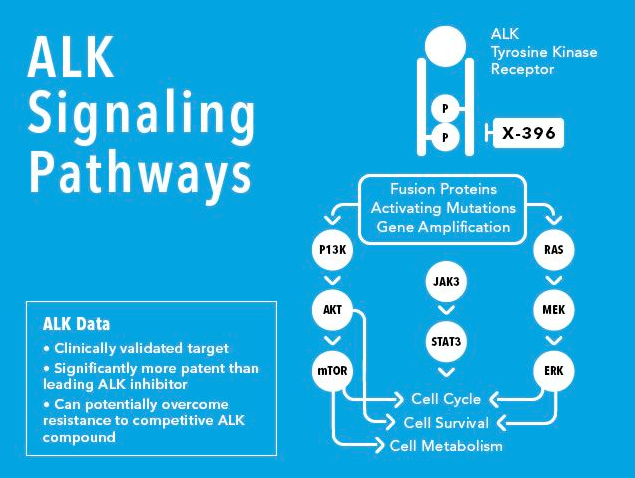
鹽酸恩沙替尼作用機理圖
此次鹽酸恩沙替尼(X-396)申報藥品注冊依據的是“評價X-396膠囊治療克唑替尼耐藥的間變性淋巴瘤激酶(ALK)陽性非小細胞肺癌患者療效和安全性的Ⅱ期單臂、多中心臨床研究”,研究結果顯示鹽酸恩沙替尼對克唑替尼耐藥的ALK陽性非小細胞肺癌患者(NSCLC)具有良好的療效和安全性。在療效性方面,恩沙替尼整體ORR為52.6%,疾病控制率為87.8%,中位PFS為11.2個月,顱內ORR為71.4%,顱內病灶控制率達95.2%。此前,公司披露了截至2018年9月中旬的臨床研究數據,獨立評審委員會(IRC)評估的整體ORR為48.7%,疾病控制率為87.8%,中位PFS為9.7個月,顱內ORR為66.7%,顱內病灶控制率達92.8%,整體療效和顱內療效均達到預期指標。兩相對比,五項數據除一項持平外其他均有更好提升,整體療效和顱內療效均顯示出良好的持續性結果。在安全性方面,臨床研究顯示安全耐受性良好,最常見的不良反應為皮疹和ALT升高、AST升高,大多為輕中度,經暫停用藥和/或對癥治療等可恢復或緩解,提示鹽酸恩沙替尼具有良好可控的安全性。
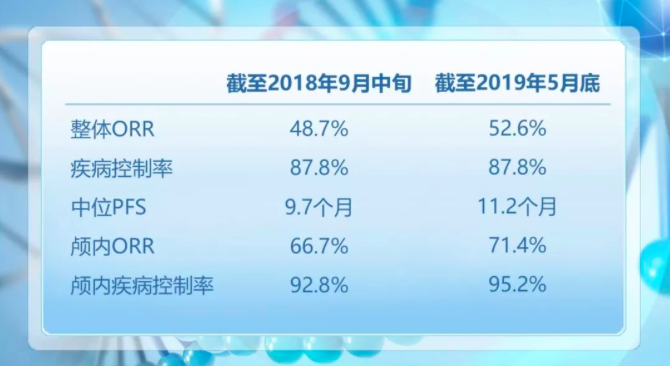
鹽酸恩沙替尼藥品注冊臨床試驗數據
鹽酸恩沙替尼是貝達和控股子公司Xcovery Holdings,Inc.共同開發的全新的、擁有完全自主知識產權的化合物,是一種新型強效、高選擇性的新一代ALK抑制劑。去年12月份,鹽酸恩沙替尼用于此前接受過克唑替尼治療后進展的或者對克唑替尼不耐受的ALK陽性的局部晚期或轉移性非小細胞肺癌患者的藥品注冊申請獲得國家藥監局受理。今年2月份,國家藥監局藥品審評中心(CDE)將其納入優先審評程序。目前,公司正在遞交補充材料,配合CDE的進一步審評工作。公司同時在國內外就鹽酸恩沙替尼開展了多項臨床研究,其中一線治療ALK陽性NSCLC患者的全球多中心III期臨床試驗正在順利推進中,屆時有望成為第一個由中國公司主導的在全球同步上市的自主創新藥。
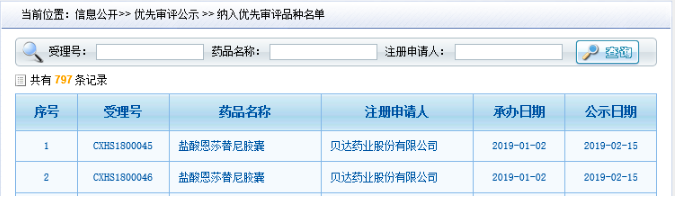
CDE網站公示信息
公司資深副總裁兼首席醫學官毛力教授表示,臨床研究數據充分證明,鹽酸恩沙替尼在療效上與進口藥相比更有優勢,特別在顱內轉移患者中有更高的應答率,而且安全性更優,可為ALK陽性的NSCLC患者提供一種新的有效的治療方案選擇。貝達將繼續做好相關上市準備工作,期待鹽酸恩沙替尼能夠盡早上市,滿足更多肺癌病人的臨床需求,造福更多患者。
關于鹽酸恩沙替尼
鹽酸恩沙替尼是一種新型強效、高選擇性的新一代ALK抑制劑,是貝達藥業和控股子公司Xcovery共同開發的全新的、擁有完全自主知識產權的創新藥,用于接受過克唑替尼治療后進展的或者對克唑替尼不耐受的ALK陽性的局部晚期或轉移性非小細胞肺癌患者提供新的治療。目前尚無針對該靶點的國產創新藥物上市,鹽酸恩沙替尼的上市將填補國內空白。
關于貝達藥業
貝達藥業(300558.SZ)是一家由海歸高層次人才團隊創辦,以自主知識產權創新藥物研究和開發為核心,集研發、生產、營銷于一體的國家級高新技術企業。自主研發了中國第一個小分子靶向抗癌藥——鹽酸埃克替尼(商品名:凱美納),被譽為堪比民生領域“兩彈一星”的重大突破,兩獲中國專利金獎,斬獲我國化學制藥行業第一個國家科技進步一等獎。截至目前,埃克替尼已惠及22萬多名晚期肺癌患者,累計銷售達65億元。公司建立了完整的新藥研發體系,在杭州、北京分別設有研發中心,在研創新藥30余項,涵蓋了肺癌、腎癌、乳腺癌等多個腫瘤適應癥。公司還先后與Amgen、Xcovery、Tyrogenex、Merus、天廣實、益方生物等國內外領先的制藥企業達成戰略合作,為促進全人類的健康福祉而共同努力。
下一條: 喜訊!貝達藥業BPI-16350項目I期臨床研究第一例受試者入組
