
9月2日,貝達藥業鹽酸恩沙替尼全球開放多中心隨機對照Ⅲ期一線臨床研究(eXalt 3 研究)在國際頂級醫學期刊《美國醫學會雜志·腫瘤學》(JAMA Oncology,影響因子為31.777)上發表。
鹽酸恩沙替尼(商品名:貝美納?)是貝達藥業和控股子公司Xcovery共同開發的全新的、擁有完全自主知識產權的創新藥,2020年11月恩沙替尼二線治療適應癥獲批上市,成為中國第一個用于治療ALK突變晚期非小細胞肺癌的國產1類新藥,填補了同類藥物國產空白。2021年,公司基于eXalt 3研究結果申報了恩沙替尼一線治療適應癥,并于今年8月被國家藥品監督管理局納入優先審評。
eXalt 3 研究是一項全球開放多中心隨機對照Ⅲ期臨床研究,旨在評估恩沙替尼對比克咗替尼對未經過治療的(一線)攜帶ALK陽性NSCLC患者治療的療效和安全性。研究全球牽頭PI為美國范德堡大學Leora Horn教授,中國牽頭PI是廣東省人民醫院吳一龍教授。2021年9月2日,eXalt 3研究數據首次公開發布的結果(數據截止日期為2020年7月1日)發表于JAMA Oncology,證實了首個國產ALK TKI恩沙替尼超越進口同類藥,成為ALK陽性NSCLC患者全新的治療選擇。
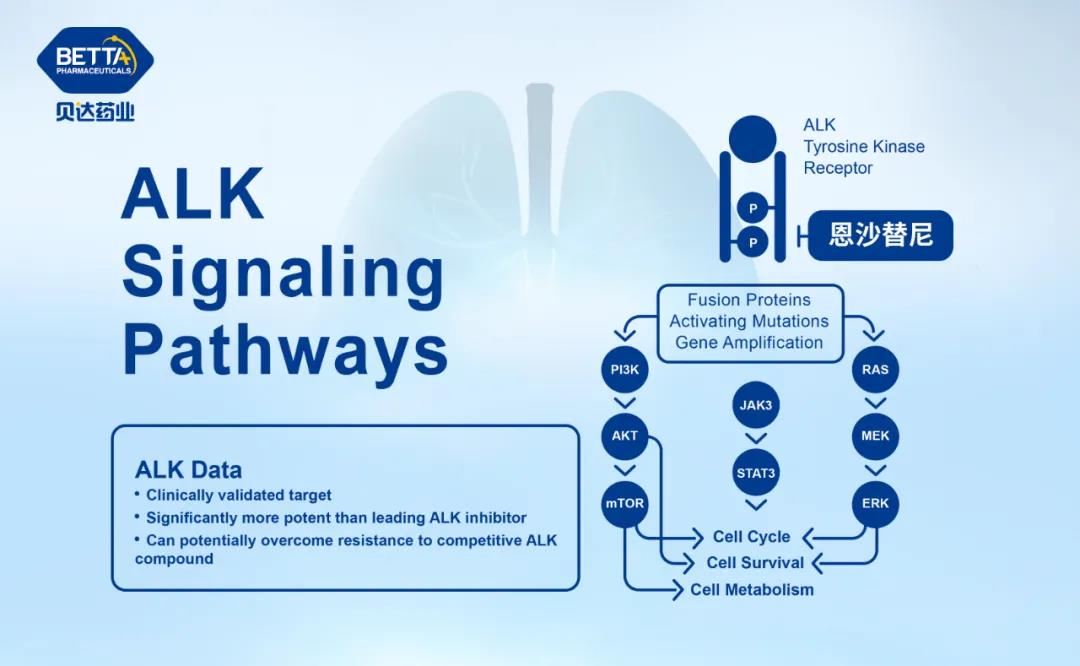
△鹽酸恩沙替尼作用機理圖
廣東省人民醫院吳一龍教授表示,我們在JAMA Oncology發表的恩沙替尼一線數據的是非常確切扎實的,根據這個結果來申請恩沙替尼一線適應癥具有信心。此外,文章中提出了mITT人群的PFS的概念,這為后續的臨床研究提供了重要的借鑒意義:在未來的臨床研究中,要盡可能采用國家批準并且質量得到驗證的檢測方法進行檢測,避免假陽性和假陰性給試驗結果帶來影響。希望貝達藥業的恩沙替尼能夠借鑒埃克替尼十年來的成功經驗,更好地解決臨床問題。
貝達藥業董事長兼首席執行官丁列明博士表示,截止到2021年8月,恩沙替尼累計發表SCI文章共15篇,影響因子累計138.613。此次恩沙替尼全球一線研究數據在國際權威期刊JAMA Oncology發表,充分證明了中國第一個擁有自主知識產權的ALK TKI優于進口同類藥物,為恩沙替尼的全球上市奠定了堅實基礎,也代表了國際學術界對中國醫藥創新成果的充分認可。目前,公司基于eXalt 3研究結果申報的恩沙替尼國內一線治療適應癥已經被納入優先審評,正在積極準備恩沙替尼美國一線適應癥的上市申報,期待能早日惠及全球ALK陽性NSCLC患者。
下一條: 貝達藥業凱美納和貝美納重磅亮相2021年服貿會
