12月3日,2022MSK- CTONG中美聯合研討大會(MSK- CTONG Symposium 2022)在廣州召開。會上,廣東省臨床試驗協會副會長兼秘書長、廣東省人民醫院腫瘤醫院院長周清教授發布了恩沙替尼eXalt 3 全球多中心一線臨床研究亞裔療效數據。

恩沙替尼亞裔療效數據亮點
1.亞裔基線無腦轉移人群PFS(無進展生存期)研究者評估結果為47.1個月;獨立評審評估結果尚未達到觀察終點,未來或可超越研究者評估結果。
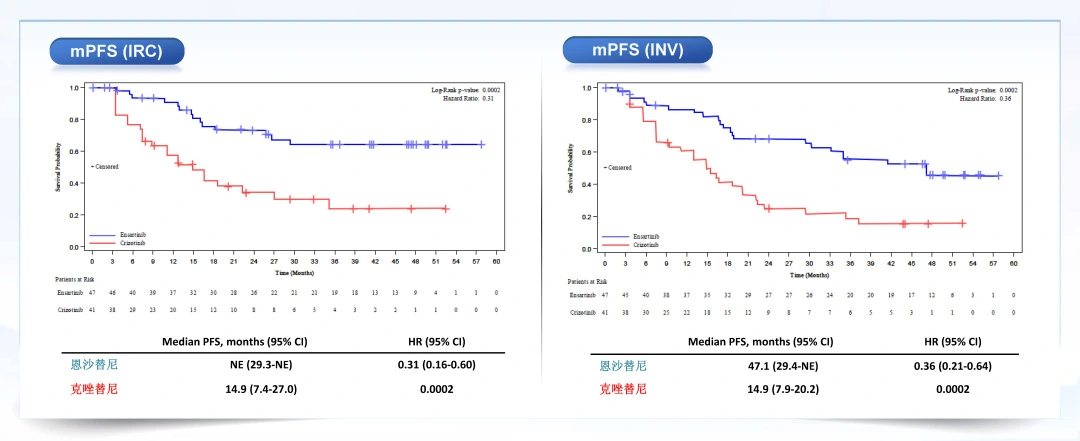
2.亞裔基線伴腦轉移人群PFS獨立評審評估結果為23.9個月。
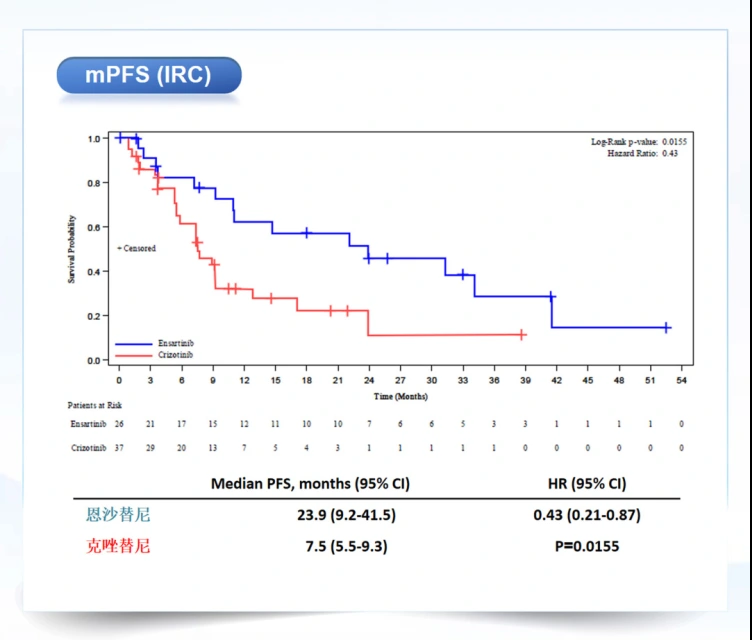
3.亞裔mITT人群PFS獨立評審評估結果為41.5個月。
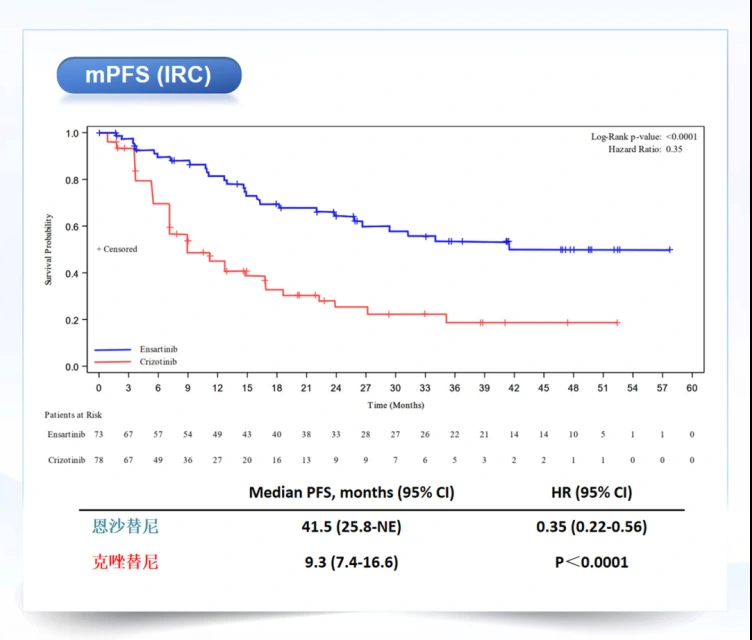
4.恩沙替尼在基線無腦轉移人群中4年OS率達75.7%;基線伴腦轉移人群4年OS率達47.7%;總體人群4年OS率達66.3%。
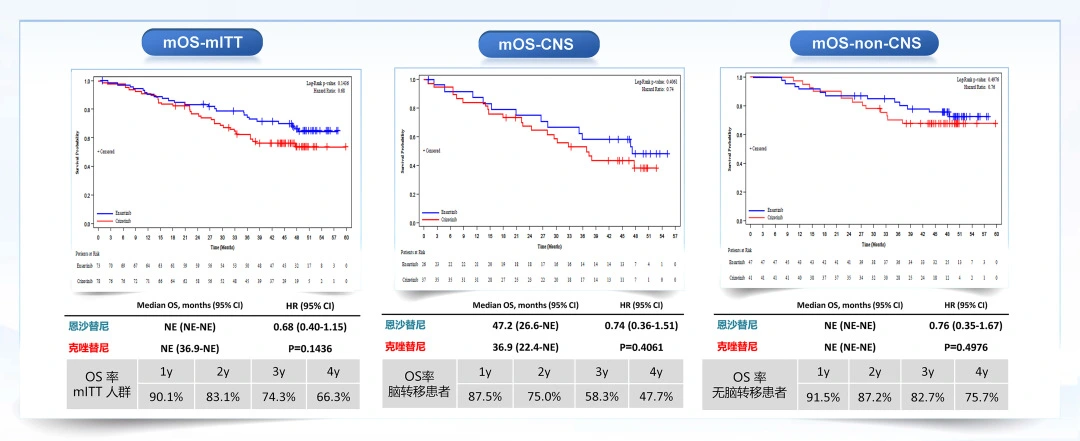
本次發布的臨床研究數據充分證明了恩沙替尼在亞裔人群中應用于一線治療,無論患者是否伴有腦轉移,均可以獲得PFS的顯著獲益且OS也表現出獲益趨勢。在基線無腦轉移人群中47.1個月的超長PFS再一次夯實了恩沙替尼是ALK陽性NSCLC患者的不二選擇。
MSK-CTONG大會結束后,恩沙替尼eXalt 3 全球多中心臨床研究中國Leading PI吳一龍教授出席了恩沙替尼亞裔數據首發新聞發布會。吳一龍教授表示:“從今天的數據發布來看,我們可以說恩沙替尼是專門為亞洲人設計的,特別是為中國人設計的ALK TKI。從數據回顧來看,恩沙替尼療效的提升沒有以犧牲安全性為代價,真正做到了療效持久也同樣安全,這也是恩沙替尼亞裔數據公布的意義。”
貝達藥業董事長丁列明博士在發布會中介紹了恩沙替尼的研發歷程,向主導研發的諸多優秀專家表示感謝,向做出巨大貢獻的患者表示敬意。他說,恩沙替尼繼去年與埃克替尼共同亮相國家“十三五”科技成就展之后,又在今年黨的二十大期間,入選“奮進新時代”主題成就展,社會各界對這個創新成果都充滿信心。
貝達藥業副總裁季東在發布會上向參與eXalt 3臨床研究的臨床科研團隊、患者及患者家屬、CRO等合作伙伴致以誠摯的感謝。
關于eXalt 3
eXalt 3 研究是一項全球開放多中心隨機對照Ⅲ期臨床研究,旨在評估鹽酸恩沙替尼對比克唑替尼對未經過治療的(一線)攜帶ALK陽性NSCLC患者治療的療效和安全性。研究全球牽頭PI為美國范德堡大學Leora Horn教授,中國牽頭PI是廣東省人民醫院吳一龍教授。研究涉及21個國家和地區的123個研究中心,全球總計入組290名患者,中國入組140名患者。
關于鹽酸恩沙替尼
鹽酸恩沙替尼(商品名:貝美納)是一種新型強效、高選擇性的新一代ALK抑制劑,是貝達藥業和控股子公司Xcovery共同開發的全新的、擁有完全自主知識產權的創新藥。2020年11月,恩沙替尼二線治療適應癥獲批上市,成為中國第一個用于治療ALK突變晚期非小細胞肺癌的國產1類新藥,填補了同類藥物國產空白,有望成為首個由中國企業主導在全球上市的肺癌靶向創新藥。2021年12月,恩沙替尼被納入國家醫保目錄。2022年3月,公司基于eXalt 3研究結果申報的恩沙替尼一線治療適應癥獲批上市,4月,恩沙替尼術后輔助治療獲批開展臨床試驗。目前正積極準備一線適應癥的國談。
下一條: 喜訊!貝達藥業兩項產品榮獲2022“健康中國?21CC”優秀案例
