近日,貝達藥業收到國家藥品監督管理局簽發的《受理通知書》(受理號:CXSL2200622國)公司申報的BPB-101雙抗注射液臨床試驗申請已獲得國家藥品監督管理局受理。
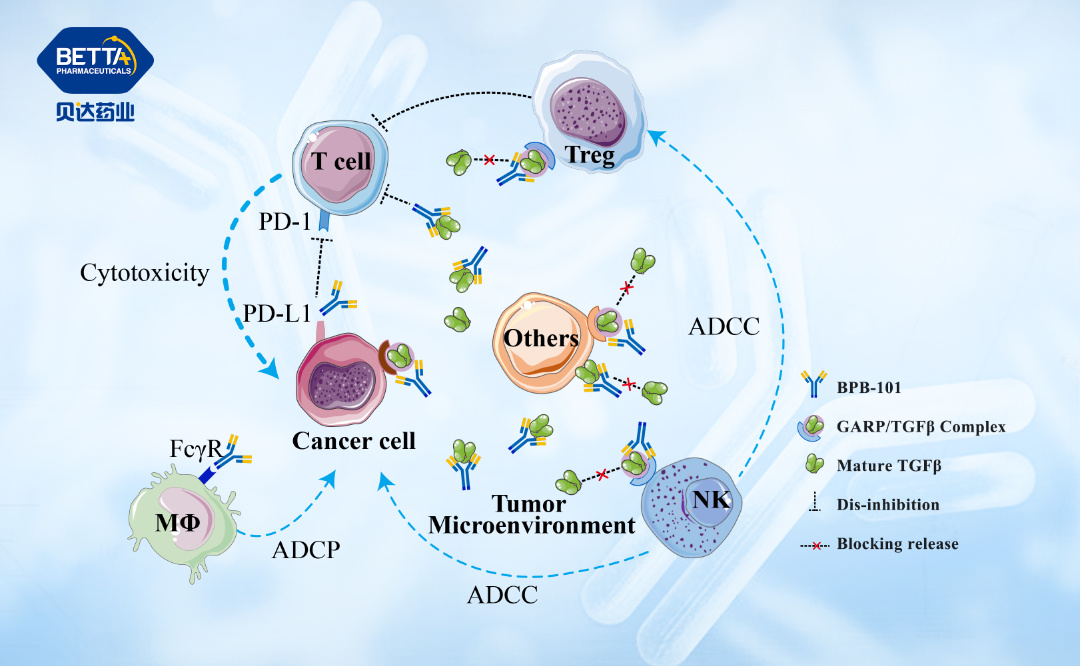
△BPB-101作用機理圖
BPB-101雙抗注射液是由貝達藥業自主研發的第一款全新的、擁有完全自主知識產權的First-in-class (FIC) 大分子新藥,具有三功能的雙特異性IgG1亞型人源化抗體。本品擬用于多種晚期實體瘤,包括但不限于非小細胞肺癌、卵巢癌、乳腺癌、食管癌、黑素瘤、子宮內膜癌、膀胱癌、膽管癌、結直腸癌、肝癌等癌癥患者的治療。
臨床前研究顯示,BPB-101可以特異性靶向GARP-TGF-β復合體、成熟的TGF-β以及PD-L1,進而解除腫瘤微環境TGF-β信號軸和PD-1/PD-L1信號軸的雙重免疫抑制,恢復并增強免疫細胞對腫瘤細胞的殺傷功效,從而抑制腫瘤的生長和存活。

△大分子生物部團隊
貝達藥業免疫學高級總監徐汶新博士表示,腫瘤微環境是惡性腫瘤細胞生長、繁殖、轉移和侵襲的重要“庇護場所”。在腫瘤微環境中,PD-L1/PD-1信號軸和TGF-β信號軸是互補的,非冗余的免疫抑制信號通路。 同時抑制兩種信號通路,不但可以恢復并增強免疫細胞對腫瘤細胞的殺傷,增加患者的整體獲益,也可對引發耐藥的旁路激活途徑產生聯合抑制作用。BPB-101可以特異性地結合GARP-TGF-β或SLC復合體,封閉產生TGF-β的源頭,同時,也可特異性地中和腫瘤微環境中已經成熟的TGF-β,徹底清除TGF-β軸的抑制。BPB-101優異的PD-L1單域抗體靶端,特異性地阻斷了PD-1/PD-L1 和CD-80/PD-L1形成的免疫抑制作用。 此外,BPB-101也可以抑制Treg細胞的負向調節功能,增強免疫效應細胞的抗腫瘤功效。這些特征表明,BPB-101是和現有的PD-(L)1/TGF-β(R)類或GARP抗體類不同的藥物分子,是個廣譜的抗腫瘤藥物,對眾多種實體腫瘤均有廣闊的臨床應用前景。
貝達藥業資深副總裁兼首席科學家王家炳博士表示,BPB-101治療性雙特異性抗體已通過充分的臨床前研究和安全性評估,并展現出了優秀的體內外藥效活性,良好的藥代動力學及安全性特征。作為公司自主研發的第一款全新的、擁有完全自主知識產權的FIC大分子新藥,有望為更多患者帶來更好的治療選擇,進一步增強公司在腫瘤治療領域的影響力,期待該項目有更多研究成果,早日上市惠及更多患者。
下一條: 貝達藥業HIF-2α抑制劑BPI-452080藥品獲批開展臨床試驗
